Kultivert kjøtt er dyrt, men kostnadene synker. Den største hindringen? Vekstmedier, som kan koste hundrevis av pund per liter. For å konkurrere med tradisjonelt kjøtt, må prisene falle til £1 per liter eller mindre. Tre strategier driver denne endringen:
- Cell Line Engineering: Justering av dyreceller for å redusere næringsbehov og vokse effektivt.
- Media Optimalisering: Erstatte kostbare farmasøytiske ingredienser med billigere matvarealternativer.
- Bioreaktor Forbedringer: Skalere produksjonen med større, mer effektive systemer.
Hver tilnærming tar for seg en unik utfordring, men deres samlede fremgang er nøkkelen til å gjøre kultivert kjøtt rimelig. Målet? Å bringe prisene nærmere konvensjonelt kjøtt, og gjøre det tilgjengelig for alle.
Ingeniørkunst av cellelinjer for kultivert kjøtt og bærekraftig cellulær landbruk #culturedmeat
1. Cell Line Engineering
Cell line engineering tilbyr en smart måte å redusere næringskostnader på ved å justere dyreceller for å produsere sine egne vekstfaktorer. I stedet for å stadig tilsette dyre vekstfaktorer til kulturmediet, gjør forskere cellene i stand til å lage disse næringsstoffene selv gjennom autokrin signalering.
I 2024 klarte Andrew J. Stout og hans team ved Tufts University å konstruere bovine muskelceller til å produsere sin egen FGF2 [4][2]. Kevin Kayser, Chief Scientific Officer hos Upside Foods, oppsummerte tilnærmingen perfekt:
"La oss bygge en prosess og deretter velge en cellelinje som gjør det vi ønsker at den skal gjøre. Det vil være mye mer arbeid i starten, men til slutt vil det oversettes til bedre kostnader" [1].
Kostnadsreduksjonspotensial
Rekombinante proteiner og vekstfaktorer er de største kostnadsdriverne i produksjonsprosessen [3]. Ved å konstruere celler til å generere sine egne vekstfaktorer, kan selskaper eliminere behovet for kostbare eksterne tilskudd - noe som ellers ville kreve en kostnadsreduksjon på nær 99% for å gjøre dyrket kjøtt kommersielt levedyktig [5]. I tillegg gjør det å modifisere celler til å vokse i suspensjon, i stedet for å kreve en overflate, det mulig å bruke massive omrørte bioreaktorer (noen som overstiger 20 000 liter), noe som betydelig øker produksjonseffektiviteten [2].
Implementeringstidspunkt
Denne tilnærmingen er ikke uten sine utfordringer.Utvikling og karakterisering av en ny cellelinje tar vanligvis 6 til 18 måneder [3], noe som står i skarp kontrast til den mye kortere produksjonssyklusen på bare 2–8 uker, fra cellebank til høsting [3]. Innen 2023 var nesten halvparten av dyrkede kjøttbedrifter allerede i gang med å utforske genetisk ingeniørkunst for enten forsknings- eller kommersielle formål [3], noe som posisjonerer industrien til å ytterligere forbedre kostnadsbesparende strategier.
Tekniske Utfordringer
Det er fortsatt hindringer å overvinne. Å opprettholde genomisk stabilitet og oppnå udødelighet for ubegrenset celleproliferasjon - samtidig som man sikrer at cellene fortsatt kan differensiere riktig - forblir en vanskelig nøtt å knekke [4][3]. I tillegg er tilgjengeligheten av cellelinjer med de riktige egenskapene fortsatt begrenset [4].Disse utfordringene fremhever kompleksiteten i cellelinjeingeniørkunst, men de potensielle belønningene gjør det til en lovende vei for å redusere kostnader. Neste, vil vi utforske strategier for optimalisering av medier.
2. Optimalisering av medier og vekstfaktorer
Å redusere kostnadene for vekstmedier er en nøkkelstrategi for å gjøre dyrket kjøtt mer rimelig. Akkurat nå er cellekulturmedier den største utgiften i produksjon av dyrket kjøtt [5][3]. Ved å kutte ned disse kostnadene, er det en stor mulighet til å bringe prisene nærmere det forbrukerne er villige til å betale.
For å nå en målpris på £8 per kilogram, må mediekostnadene reduseres med over 99,9% fra dagens farmasøytiske nivåer. Vekstfaktorer alene må begrenses til bare £0,80 per kilogram [3][5].Som Good Food Institute forklarer:
"Den største utfordringen den kultiverte kjøttindustrien står overfor er ikke bare å unngå dyre komponenter i cellekulturmediet, men heller å finne ut hvordan man kan gjøre det på en kostnadseffektiv måte og hvordan man kan optimalisere rimelige formuleringer for maksimal produktivitet" [3].
Kostnadsreduksjonspotensial
En av hovedmetodene for å kutte kostnader er å erstatte dyre farmasøytiske ingredienser med billigere, matvarekvalitetsalternativer. For eksempel, albumin, som utgjør 96,6% av rekombinant proteinbehov, blir målrettet med plantebaserte substitutter som raps og kikerter. På samme måte bytter selskaper ut individuelle aminosyrer med mer rimelige plantehydrolysater [5][3][1].
Fremgang blir allerede gjort.I august 2024 introduserte Believer Meats et medium uten dyrekomponenter som koster bare £0,50 per liter [6]. Ved å bruke kontinuerlige produksjonsmetoder som tangentiell strømfiltrering, viste deres analyse at dyrket kylling kunne produseres til £5 per pund i en 50 000-liters anlegg - noe som gjør det konkurransedyktig med priser på økologisk kylling [6]. På samme måte demonstrerte Mosa Meat, i samarbeid med Nutreco, at det å bytte fra legemiddelgrad til matgrad aminosyrer alene kunne kutte kostnadene med en faktor på 100, alt uten å ofre celleutbytte [1].
Implementeringstidspunkt
Sammenlignet med cellelinjeingeniørkunst kan medieoptimalisering levere resultater mye raskere.Mens utviklingen av nye cellelinjer kan ta 6 til 18 måneder [3], utnytter omformulering av medier ofte eksisterende matvarekjedene, noe som fremskynder prosessen. Susanne Wiegel, leder for Alternative Protein Programme hos Nutreco, oppsummerer det godt:
"Å mate celler er ikke så forskjellig fra å mate dyr. Flertallet av næringsstoffene leveres gjennom landbruksavlinger" [1].
Tekniske Utfordringer
Til tross for løftet om kostnadsbesparelser, kommer bruken av matvareingredienser med utfordringer. Disse ingrediensene kan introdusere urenheter, batch-inkonsistenser og potensielle påvirkninger på celleytelse og produktkvalitet [5][2]. I tillegg er det ingen liten oppgave å skalere opp produksjonen for å møte etterspørselen.Å fange bare 1% av det globale kjøttmarkedet ville kreve millioner av kilogram rekombinant albumin - langt over dagens produksjonsnivåer for mange industrielle enzymer [5].
Neste, vil vi utforske hvordan forbedringer i bioreaktorer og prosesser kan ytterligere redusere kostnadene.
sbb-itb-c323ed3
3. Forbedringer i bioreaktorer og prosesser
Etter å ha raffinert cellelinjeingeniørkunst og optimalisert medier, ligger neste steg i å redusere kostnadene for kultivert kjøtt i å forbedre bioreaktorer og produksjonsprosesser. Mens cellelinjer og medier fokuserer på den biologiske siden, spiller de fysiske systemene - bioreaktorer og produksjonsarbeidsflyter - en avgjørende rolle i å gjøre kultivert kjøtt mer rimelig. Som Good Food Institute treffende uttaler:
"Bioprocessdesign er nøkkelen til å låse opp storskala produksjon av kultivert kjøtt" [3].
Akkurat nå er de fleste bioreaktorer som brukes i produksjon av kultivert kjøtt tilpasset fra legemiddelindustrien. Disse systemene er designet for høyverdi, lavvolumproduksjon, noe som ikke er ideelt for de kostnadseffektive, høyvolumkravene til matproduksjon [3]. For å konkurrere med tradisjonelt kjøtt, trenger industrien spesialbygde bioreaktorer designet spesielt for storskala, økonomisk produksjon. Dette er hvor prosessoptimaliseringer kan bidra til å redusere kostnadene ytterligere.
Kostnadsreduksjonspotensial
En av de mest lovende måtene å kutte kostnader på er ved å gå fra legemiddelgradert til matgradert produksjonsstandarder. I motsetning til legemiddelapplikasjoner trenger kultivert kjøtt bare å oppfylle matsikkerhetsstandarder, som er mindre strenge. Dette skiftet kan betydelig redusere driftskostnadene [3].
Prosesseffektivitet er en annen kritisk faktor.Teknikker som resirkulering av vekstmedier, ombruk av avfallsstrømmer og implementering av automatisering kan bidra til å minimere bruken av kostbare innsatsfaktorer [3]. For eksempel, i september 2023, kunngjorde Upside Foods sine planer for en kommersiell anlegg i nærheten av Chicago. Dette anlegget har som mål å produsere 13 000 tonn kultivert kjøtt årlig ved å bruke bioreaktorer så store som 100 000 liter [1]. Kevin Kayser, selskapets Chief Scientific Officer, fremhevet viktigheten av å fokusere på råvareinnsatsfaktorer:
"En av grunnene til at jeg ble ansatt var råvareinnsatsfaktorer... Da jeg først begynte, var det øverst på listen" [1].
Skalerbarhet
Å oppskalere bioreaktorer er avgjørende for å oppnå prisparitet med konvensjonelt kjøtt. For tiden bruker pilotanlegg bioreaktorer som varierer fra 100 til 1 000 liter.Imidlertid antyder techno-økonomiske analyser at oppnåelse av konkurransedyktige priser vil kreve bioreaktorer med volum på 20 000 liter eller mer - muligens til og med 100 000 liter [3][1][2]. Innen utgangen av 2024 hadde minst ett selskap lykkes med å oppskalere til bioreaktorer med en kapasitet på 15 000 liter [3].
Bransjen beveger seg gjennom distinkte faser: fra benkeskala forskning (bioreaktorer under 10 liter), til pilot-skala testing, og til slutt til industriell produksjon. Hver fase krever ikke bare større utstyr, men også innovasjoner innen blanding, oksygentilførsel og overvåkningssystemer [3].
Tekniske Utfordringer
Oppskalering av bioreaktorer er ikke uten sine utfordringer.Større bioreaktorer medfører unike tekniske utfordringer, som å håndtere skjærkrefter under blanding og oksygenering, som kan skade delikate celler [3]. Oksygentransport blir stadig mer kompleks etter hvert som volumene av bioreaktorer øker, og opprettholdelse av sterilitet i storskala, matvaregodkjente anlegg er kritisk - enhver kontaminasjon kan resultere i betydelige produksjonstap [3].
Som Kevin Kayser bemerket, utforsker industrien nytt terreng:
"Når du begynner å snakke om 100 000 L eller mer, vet jeg ikke om det vil kreve noen endring i mediet. Vi har ikke nådd det nivået" [1].
I motsetning til medieoptimalisering, som kan utnytte eksisterende matforsyningskjeder, krever skalering av bioreaktorer å løse helt nye ingeniørproblemer, spesielt på disse utenkelige størrelsene [3].
Implementeringstidspunkt
Bygging av industrielle anlegg i stor skala er en tidkrevende og kapitalintensiv prosess. Mens utviklingen av en ny cellelinje kan ta 6 til 18 måneder [3], tar konstruksjon og igangsetting av et produksjonsanlegg i full skala år med planlegging og betydelig investering [3]. Imidlertid hjelper nye teknologier med å fremskynde prosessen. For eksempel har automatiserte og skybaserte systemer vist seg å redusere utviklingssykluser med 25% og forbedre suksessratene for oppskaleringsprosesser med 30% [7]. Chris Williams, administrerende direktør i Culture Biosciences, forklarte:
"Overgangen til skybasert, modulær bioprosessering akselererer i bioteknologi- og biopharma-sektorene... Det tilbyr en fleksibel, kostnadseffektiv løsning for team som krever raskere utviklingssykluser og skalerbarhet" [7].
Selve dyrkingsprosessen - fra cellebank til høsting - tar vanligvis 2 til 8 uker, avhengig av hvilken type kjøtt som produseres [3]. Fremskritt innen bioprosessering vil være avgjørende for å gjøre dyrket kjøtt til et konkurransedyktig alternativ i markedet.
Sammenligning av de tre tilnærmingene
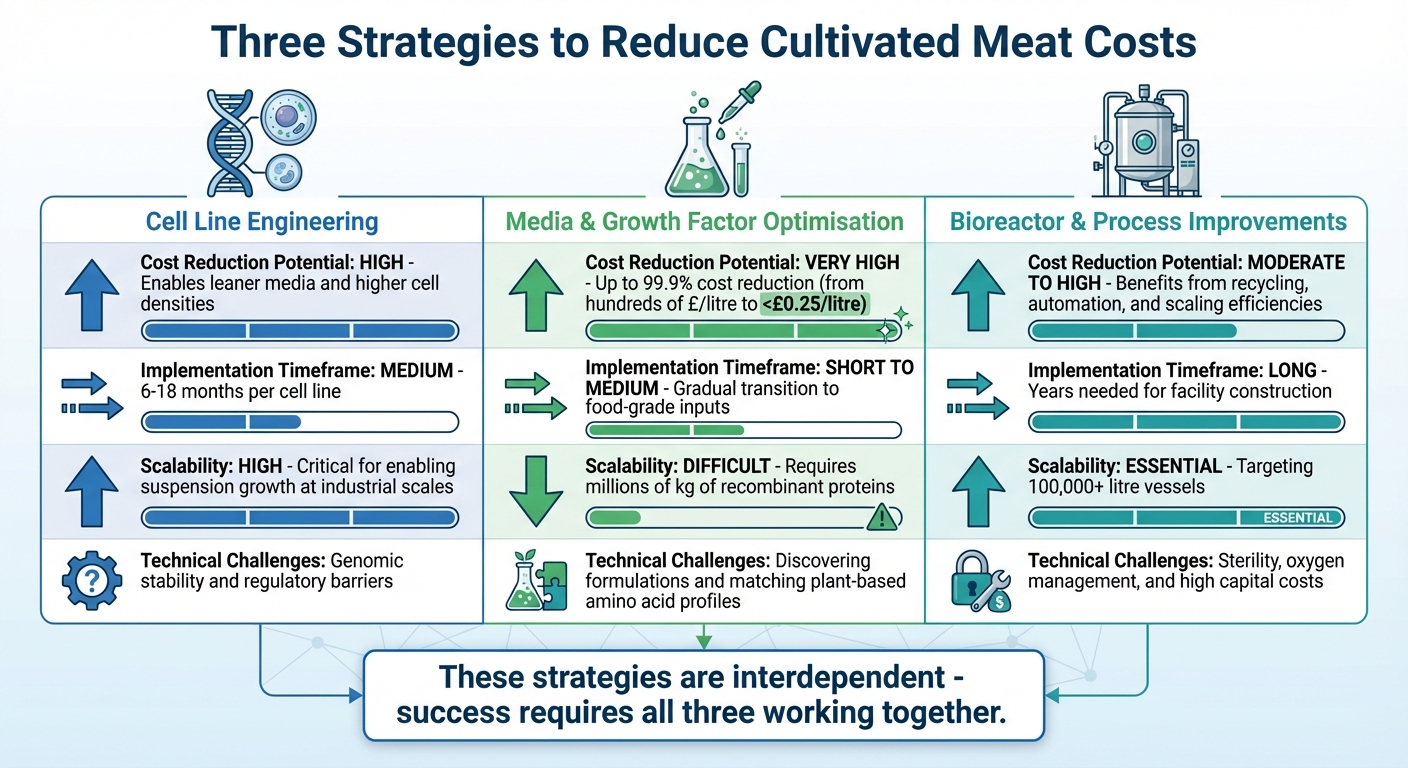
Sammenligning av tre strategier for å redusere produksjonskostnadene for dyrket kjøtt
Å se på cellelinjeingeniør, medieoptimalisering og bioreaktorfremgang på siden av hverandre avslører hvor sammenkoblede disse strategiene er. Hver av dem bringer sine egne styrker og hindringer til bordet, men sammen skaper de en vei for å redusere kostnadene i produksjonen av dyrket kjøtt.
Her er en oversikt over hvordan disse tilnærmingene sammenlignes på tvers av fire nøkkelkriterier:
| Kriterium | Cell Line Engineering | Medie &og vekstfaktoroptimalisering | Bioreaktor &og prosessforbedringer |
|---|---|---|---|
| Kostnadsreduksjonspotensial | Høy – muliggjør slankere medier og høyere celledensiteter | Veldig høy – kan kutte kostnader med opptil 99.9% fra nåværende biomedisinske priser | Moderat til Høy – fordeler fra resirkulering, automatisering og storskala effektivitet |
| Implementeringstid | Moderat – tar vanligvis 6–18 måneder per cellelinje | Kort til Moderat – involverer gradvis overgang til matvarekvalitetsinnhold | Lang – år nødvendig for anleggsbygging og idriftsettelse |
| Skalerbarhet | Høy – kritisk for å muliggjøre suspensjonsvekst i industrielle skalaer | Difficult – krever produksjon av millioner av kilogram rekombinante proteiner | Essensiell – målretter 100,000-liters+ beholdere for storskala produksjon |
| Tekniske Utfordringer | Genomisk stabilitet og regulatoriske barrierer | Oppdage formuleringer og matche plantebaserte aminosyreprofiler | Sikre sterilitet, oksygenhåndtering og håndtering av høye kapitalkostnader |
Hver strategi spiller en distinkt rolle i å takle kostnadsutfordringene ved kultivert kjøtt.
Medieoptimalisering skiller seg ut for sitt umiddelbare potensial til å kutte kostnader. Priser kan falle fra hundrevis av pund per liter til mindre enn £0,25 per liter [3]. Imidlertid er det en betydelig hindring å skalere denne tilnærmingen for å møte industrielle krav.
Cellinjeingeniørkunst, derimot, legger grunnlaget for suksess. Ved å muliggjøre suspensjonsvekst og redusere mediekrav, støtter det både medieoptimalisering og bioreaktorskala [3]. Uten pålitelige cellinjer ville fremdriften i de andre områdene stoppe opp.
Forbedringer av bioreaktorer er et langsiktig spill. Å utvikle og sette i drift anlegg som kan håndtere 100 000-liters beholdere er en skremmende oppgave, men det er avgjørende for å skalere opp til produksjon på råvare nivå [3].De ingeniørmessige utfordringene her, spesielt rundt sterilitet og oksygenoverføring, forblir stort sett uutforsket territorium på denne skalaen.
Virkeligheten er at ingen enkelt tilnærming kan bære vekten av kostnadsreduksjon alene. Disse strategiene er dypt sammenhengende. For eksempel har rimelige medier bare verdi hvis bioreaktorer kan operere i høye volumer, og store bioreaktorer gir bare mening hvis mediene de bruker er kostnadseffektive [3]. Sammen skaper disse innsatsene et sammenhengende rammeverk som er kritisk for å gjøre kommersielt skalert kultivert kjøtt til en realitet.
Konklusjon
Cellinjeingeniørkunst spiller en nøkkelrolle i å drive suksessen til både medierefinerings- og bioreaktorfremdrift. Ved å utvikle celler som vokser raskere, når høyere tettheter og presterer godt i magrere medier, reduserer det betydelig kostnadene knyttet til næringsstoffer og bioreaktorkapasitet.Dette gjør det til en hjørnestein i å redusere produksjonskostnader.
Medieforfining gir umiddelbare besparelser, med potensial til å kutte mediekostnader med så mye som 99,9%, og bringe priser på farmasøytisk nivå ned til mindre enn £0,20 per liter [3]. Imidlertid avhenger disse besparelsene av cellelinjer som kan trives på slike kostnadseffektive medier. Samtidig baner avanserte bioreaktordesign veien for storskala produksjon, men deres økonomiske levedyktighet avhenger av å kombinere dem med rimelige medier og robuste, konstruerte cellelinjer.
Tidslinjen for å oppnå prisparitet med premium konvensjonelt kjøtt i Storbritannia vil bli formet av hvor raskt disse tre strategiene - celleingeniørkunst, medieutvikling og bioreaktorskala - fremmes sammen. Fremgang på disse områdene vil danne grunnlaget for å gjøre kultivert kjøtt mer tilgjengelig.
For britiske forbrukere vil utbredt tilgjengelighet også avhenge av regulatorisk godkjenning, som fortsatt er under vurdering per slutten av 2025 [3], og opprettelsen av storskala produksjonsanlegg. Selskaper planlegger allerede 100 000-liters bioreaktorer og sikter mot anlegg som kan produsere opptil 13 000 tonn årlig [1], noe som signaliserer at den nødvendige infrastrukturen tar form.
Veien til rimelig kultivert kjøtt vil avhenge av sømløs integrering av disse tre strategiene. Et produksjonsøkosystem som kombinerer konstruerte celler, lavkostmedier og bioreaktorer i industriell skala vil avgjøre når kultivert kjøtt går fra nisjemåltider til hverdagslige supermarkedtilbud.
Ofte stilte spørsmål
Hvordan hjelper cellelinjeteknologi med å senke kostnadene for dyrket kjøtt?
Fremskritt innen cellelinjeteknologi har redusert kostnadene for produksjon av dyrket kjøtt ved å forbedre ytelsen til cellene som brukes i prosessen. Disse spesialdesignede cellelinjene vokser raskt, kan trives i tette miljøer, og tåler tøffe forhold som lave oksygennivåer og mekanisk stress. Dette betyr mindre avhengighet av kostbart vekstmedium og mer effektiv, høyavkastningsproduksjon i bioreaktorer.
Ved å kutte ned på råvare- og behandlingskostnader, bidrar cellelinjeteknologi til å gjøre dyrket kjøtt mer tilgjengelig. Denne fremgangen er et skritt mot å etablere det som et praktisk alternativ til tradisjonelt kjøtt.
Hva er de viktigste utfordringene ved bruk av matgodkjente medier for produksjon av dyrket kjøtt?
Overgangen til matgodkjente medier for produksjon av dyrket kjøtt medfører noen tøffe utfordringer.En av de største hindringene er kostnadene. Akkurat nå utgjør vekstfaktor-rik media - som er essensielt for cellevekst - mer enn halvparten av produksjonskostnadene. For å redusere kostnadene må produsentene gå fra dyre farmasøytiske ingredienser til billigere, matkompatible alternativer. Men her er utfordringen: utviklingen av disse rimelige alternativene, enten gjennom presisjonsfermentering eller plantebaserte metoder, er fortsatt i sine tidlige dager og krever mye investering.
Et annet stort problem ligger i å oppfylle strenge mattrygghetsstandarder. Matkvalitetsmedia må produseres under sterile forhold, fri for kontaminanter, og oppfylle EUs matforskrifter. Dette legger lag av kompleksitet til forsyningskjeder og kvalitetskontrollprosesser. I tillegg skaper fjerning av serum - som vanligvis brukes i forskningskvalitetsmedia - nye utfordringer innen avfallshåndtering.Uten serum som fungerer som en naturlig buffer, blir opphopning av biprodukter et problem, som krever avanserte resirkulerings- eller fjerningssystemer.
Det er også spørsmålet om celleadaptasjon. Mange cellelinjer, opprinnelig utviklet for serumbaserte miljøer, sliter med å vokse i kjemisk definerte, dyrefrie medier. Dette kan føre til langsommere vekst eller svakere celler, som ofte krever genetiske justeringer av cellelinjene eller opprettelse av spesialiserte kosttilskudd. Å takle disse utfordringene er avgjørende for å skalere opp produksjonen av kultivert kjøtt og gjøre det mer rimelig og tilgjengelig for forbrukerne. Hvis du er nysgjerrig på å lære mer om dette fascinerende feltet, tilbyr
Hvordan hjelper storskala bioreaktorer med å gjøre kultivert kjøtt mer rimelig?
Storskala bioreaktorer, spesielt de med kapasitet over 20 000 liter, spiller en nøkkelrolle i å senke produksjonskostnadene for kultivert kjøtt.Disse systemene muliggjør produksjon av store mengder kjøtt, noe som bidrar til å spre utgifter som utstyr, arbeidskraft og vekstmedier over et større utbytte. Denne tilnærmingen hjelper med å oppnå stordriftsfordeler, og bringer kultivert kjøtt nærmere prisen på tradisjonelt kjøtt.
Med dette produksjonsnivået kan produsentene dramatisk redusere kostnaden per kilogram, noe som baner vei for at kultivert kjøtt kan bli et mer rimelig og levedyktig alternativ for forbrukerne.













